Wirkprinzip von ADCs
ADCs sind Antikörper-Wirkstoff-Konjugate (Antibody Drug Conjugates), die die Spezifität von Antikörpern mit der Wirkung von Toxinen verbinden. Antikörper erkennen Zielstrukturen (Antigene) auf der Oberfläche von Krebszellen und binden daran. Diese spezifischen Antikörper werden mittels einer chemischen Verbindung (Linker) mit Toxinen verbunden und das daraus entstandene Konjugat führt das Toxin direkt zur Krebszelle, wo das Toxin internalisiert wird. In der erkrankten Zelle wird das Toxin freigesetzt und zerstört die Zelle.
ADCs versprechen großes Potenzial in der Krebstherapie, weil sie gezielt Krebszellen vernichten können. Das therapeutische Fenster von ADCs, d.h. das Verhältnis von Wirksamkeit und Sicherheit, ist im Vergleich zu anderen Therapieformen vorteilhaft. Da die Technologie sehr spezifisch ist, also direkt an der Krebszelle wirkt, können systemische Auswirkungen minimiert und Nebenwirkungen vermieden werden. Darüber hinaus können ADCs auch auf ruhende Zellen und bei Patienten, die auf keine Behandlung mehr ansprechen, wirken.
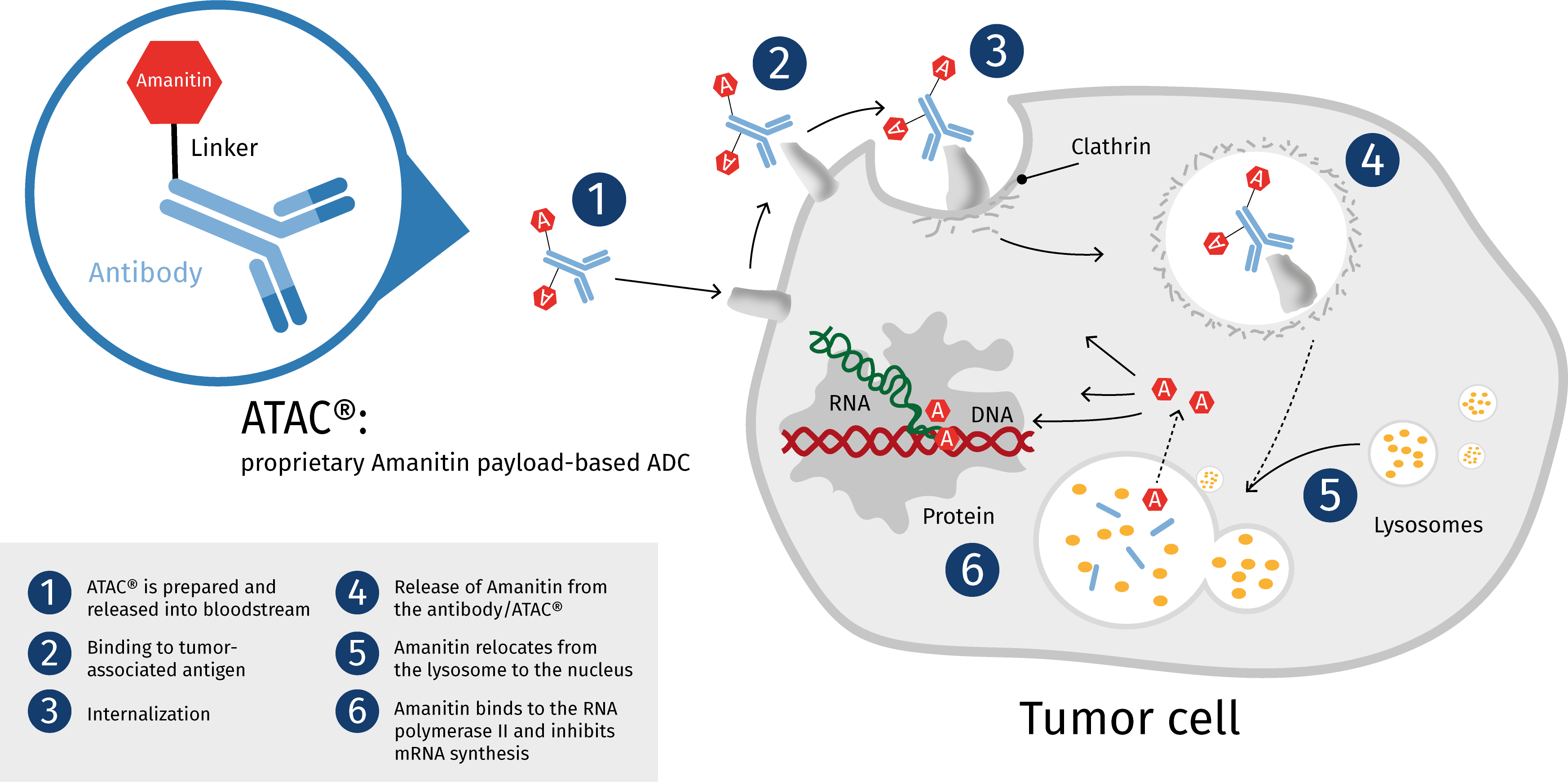
Amanitin als innovativer Wirkstoff zur Krebstherapie
Heidelberg Pharma arbeitet seit einigen Jahren an einer eigenen Technologie für Antikörper-Wirkstoff-Konjugate, den sogenannten ATACs. ATACs sind ADCs, welche auf der ATAC-Technologie beruhen und deren Beladung aus Amatoxin-Molekülen besteht. Das Unternehmen will Amanitin erstmals für die Krebstherapie zugänglich machen. Amanitin hat ein einzigartiges biologisches Wirkprinzip, auf dessen Grundlage möglicherweise hoch wirksame innovative Arzneimittel entwickelt werden können. Amanitin gehört zu einer Gruppe von natürlich vorkommenden Giften, den Amatoxinen, welche unter anderem im Grünen Knollenblätterpilz (Amanita phalloides) vorkommen.
Die Wirkung besteht in der Hemmung der RNA-Polymerase II, was bei Zellen zum sogenannten programmierten Zelltod (Apoptose) führt. Alle anderen bisher verwendeten Chemotherapeutika auch bei anderen ADCs sind in ihrer Wirkung entweder sogenannte Spindelgifte (Tubulin-Inhibitoren) oder wirken über die DNA, was sie abhängig von der Zellteilung macht. Die Hemmung der RNA-Polymerase II ist ein für die Krebstherapie neues Wirkprinzip und birgt die Chance, Therapieresistenzen zu durchbrechen oder auch ruhende Tumorzellen zu vernichten, was zu erheblichen klinischen Fortschritten führen könnte.
ATACs sind ADCs der dritten Generation, die sich durch eine verbesserte Wirksamkeit auch auf ruhende Tumorzellen auszeichnen. Ruhende Tumorzellen können mit bisherigen Standardtherapeutika kaum erreicht werden und tragen zu Tumorrezidiven und Resistenzbildung bei. Mit den ATACs sollen auch Tumore behandelt werden, die aufgrund von Therapieresistenzen nicht mehr auf eine Standard-Chemotherapie oder auf anti-tumorale Antikörper ansprechen.
YOUTUBE-Video: Prof. Andreas Pahl erklärt die ATAC-Technologie (2016; in Englisch) Link
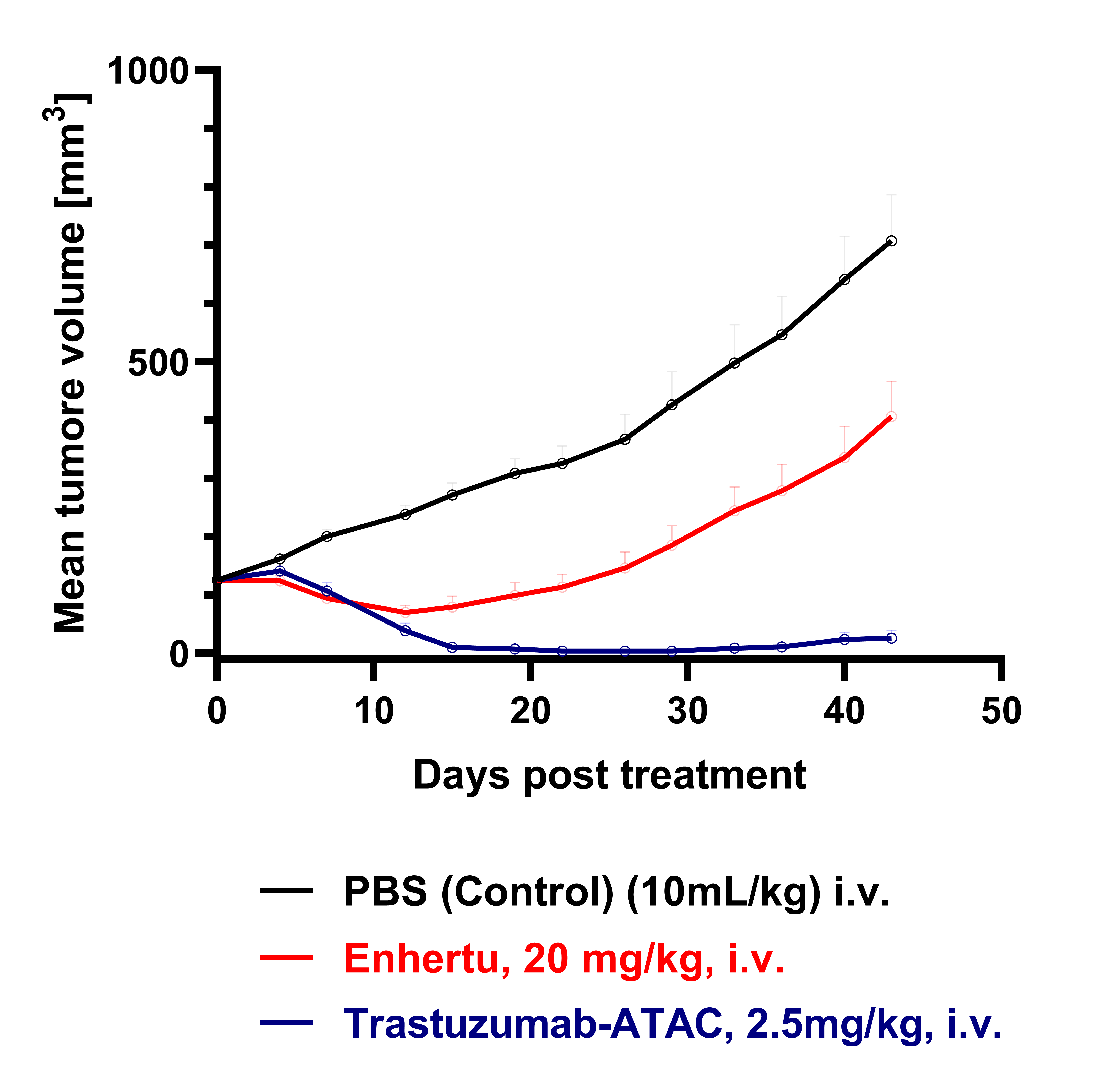
Wirksamkeit eines HER2-ATACs in einem Brustkrebs-Tiermodell im Vergleich mit Enhertu
- Ein gegen das Zielmolekül HER2 auf der Krebszelle gerichtetes ATAC wurde mit dem bereits zugelassenen HER2-Dxd-ADC (Enhertu®) verglichen.
- Das HER2-ATAC zeigte eine komplette Remission des Tumors.
Aufbau einer eigenen ATAC-Pipeline
Der Aufbau einer eigenen Pipeline steht im Fokus der Aktivitäten von Heidelberg Pharma. Grundlage dafür sind erfolgreiche Einlizenzierungen von Antikörpern und vielversprechende präklinische Daten, die mit den hergestellten ATACs generiert wurden. Diese bisherigen Daten untermauern die Erwartung, dass sich die Vorteile der auf Amanitin beruhenden Produkte auch in spezifischen ATACs für unterschiedliche Krebsindikationen bestätigen werden. Details zu unseren ATAC-Kandidaten finden Sie hier.

